产品详情
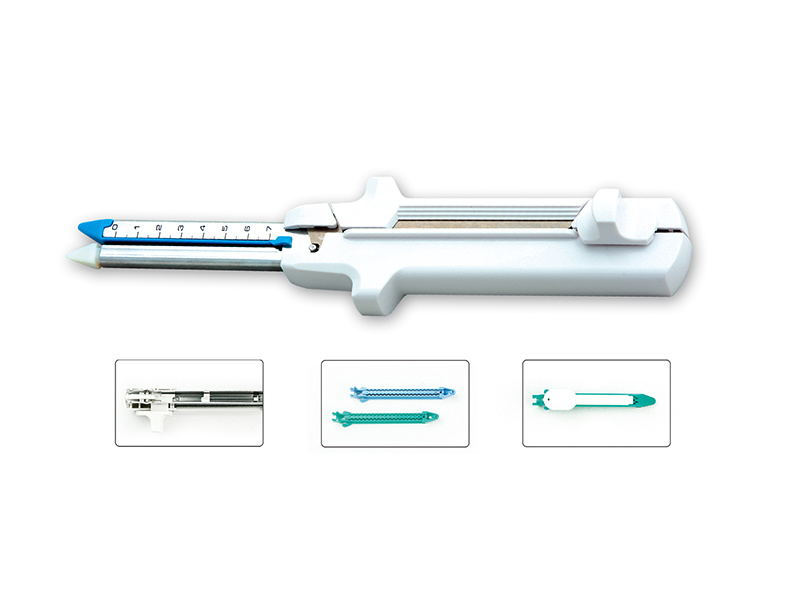
【产品名称】一次性腔镜用五排钉直线型切割吻合器及切割组件
【产品型号规格】吻合器:WNHM
切割组件:WNHZ-45A1、WNHZ-45B1、WNHZ-45E1、WNHZ-45F1、WNHZ-45G1
WNHZ-45A2、WNHZ-45B2、WNHZ-45E2、WNHZ-45F2、WNHZ-45G2
WNHZ-60A1、WNHZ-60B1、WNHZ-60E1、WNHZ-60F1、WNHZ-60G1
WNHZ-60A2、WNHZ-60B2、WNHZ-60E2、WNHZ-60F2、WNHZ-60G2
【性能指标】
1、性能:一次性腔镜用五排钉直线型切割吻合器及切割组件外形光滑、轮廓清晰,无毛刺、划伤、锈迹等缺陷。吻合器开闭应灵活,不应有卡阻现象。吻合器的复位拉钮拉回底部时能完全复位。吻合器应具有良好的吻合和切割性能,每次吻合后切割边缘整齐、无毛边。吻合后的吻合口应能承受不小于3.6kPa压力,在15s内漏水不超过10滴。切割刀刃口应锋利,切割力应不大于0.80N。吻合器具有空钉仓安全保护装置。钉仓组件与器身连接后应牢固,能承受30N的拉力不松 1、中心杆 2、金属外套管 3、转向旋钮 4、转向手柄 5、保险按钮
6、复位拉钮 7、卸载按钮 8、活动手柄 9、固定手柄
1、抵钉座 2、钉仓 3、钉仓支架 4、切割刀 5、吻合钉
3、材料:抵钉座、钉仓支架、切割刀采用20Cr13材料制成,固定手柄、转向手柄、转向旋钮采用ABS材料制成,复位拉钮采用PC材料制成,活动手柄、保险按钮、钉仓采用PA66材料制成,吻合钉采用TA2G材料制成。
4、尺寸:
表1 切割组件内吻合钉钉高说明 单位:mm
|
腔内切割切割组件 吻合钉钉高代号 |
钉高 |
极限 偏差 |
||
|
内 排 |
中 排 |
外 排 |
||
|
A |
4.8 |
4.8 |
4.8 |
±0.2 |
|
B |
3.5 |
3.5 |
3.5 |
|
|
E |
4.2 |
4.2 |
4.2 |
|
|
F |
4.0 |
4.5 |
5.0 |
|
|
G |
3.0 |
3.5 |
4.0 |
|
表2 腔内切割吻合器器身的基本尺寸 单位为毫米(mm)
|
器身的型号规格 |
金属外套管长度(L1) |
|
|
基本尺寸 |
极限偏差 |
|
|
WNHM |
155 |
±5.0 |
表3 腔内切割吻合器切割组件的基本尺寸 单位为毫米(mm)
|
型号规格 |
吻合长度(L) |
弯转角度(W/°) |
钉数 |
||
|
基本尺寸 |
极限偏差 |
基本尺寸 |
极限偏差 |
(个) |
|
|
WNHZ-45(A,B,E,F,G)(1,2) |
44.5 |
±2.0 |
37 |
±10 |
55 |
|
WNHZ-60(A,B,E,F,G)(1,2) |
60.5 |
37 |
±10 |
75 |
|
【适用范围】
适用于腹部外科、妇科、儿科和胸外科内视镜手术中组织的切除、横断和吻合,不用于侧侧吻合。
【使用方法】
打开吻合器或器身及组件的无菌包装取出吻合器器身及组件(此时切勿取下组件上的黄色保护盖),将吻合器头部及组件尾部的“↑”对准后下压并顺时针旋转,听到“咔”的声响表示器身及组件连接到位。
注1:当组件与器身不能顺利装配时,请确认器身上的黑色复位拉钮应已拉到器身最底部,或者检查拨盘上的转向旋钮应与器身上的焊接线平行。
注2:在组件与器身装配时,请勿提前取下组件上的黄色保护盖,否则可能产生以下后果:组件与器身可正常装配,术中可正常切割缝合;但是,缝合结束后切割刀无法复位,组件头部无法打开,导致组织无法取下。
取下组件黄色保护盖,握一下活动手柄,使组件头部闭合,通过穿刺器使器械到达所需的手术部位。
注1:若组件与器身连接后,握一下活动手柄,组件头部无法顺利闭合,说明组件与器身没有连接到位,请参考步骤6的方法,取下组件重新装配。此时如若强行硬捏,会使枪身内部齿条断裂,导致器械报废。
注2:组件与器身连接后,一定要确认组件上的“两排钉”文字标记位于器身转向旋钮的“左侧”或“右侧”,以便于在手术时确定预切除组织与“两排钉”文字标记在同一侧。(切除病变组织时,组件在体内,不容易被医生直观的看到)
向后拉动黑色复位拉钮,使组件头部打开(组件是可旋转的,可根据手术的需要拨动吻合器上的转向旋钮进行调节),使需要切除的组织能顺利的放入钉仓和抵钉座中间,调整好需被切割的组织,使之均匀展开,并保证没有夹住多余的组织。
注意:在组织放入组件的钳口时应注意组件上的“两排钉”文字标记,转动旋转手柄,确定预切除组织与“两排钉”文字标记在同一侧。
4、握紧活动手柄夹住组织后松开活动手柄,按下绿色保险按钮,开始手术操作,每握一次活动手柄向前吻合切割15mm,(按下绿色保险按钮开始切割后,必须切割到底,不可中途拉动黑色复位拉钮)具体吻合切割的位置可参考器身上黑色复位拉钮旁的黑色刻度线(或组件下部的黑色刻度线)。
注:切记按下绿色保险按钮后再击发,否则会使器身内部齿条断裂,导致器械报废。
5、吻合切割过程完成后向后拉动器身上的黑色复位拉钮,使钉仓头部放开夹住的手术组织。再次握一下活动手柄,组件头部闭合后,退出器械。
注:切割完成后,向后拉动黑色复位拉钮,切勿握住活动手柄,否则黑色复位拉钮无法向后拉动。
组件更换方法:如同台手术需更换组件,先向后拉动黑色复位拉钮使组件头部打开,再向后拉住拨盘上的蓝色卸载按钮,逆时针转动组件将其拆下,重新步骤1的操作,装上一个新的组件即可。
切割吻合完成后,取出切下的组织,将缝钉线与切割边缘间一定宽度的没有被破坏的组织切下,移送病理检查。
组件配置:切割吻合器器身可配合多种切割组件,切割组件为一次性使用产品。
【注意事项】
本产品使用时,应严格执行无菌操作规范。
医生使用前请认真阅读本使用说明书。
本产品供已受专业培训或在有相关经验医师指导下的医师使用。
使用前应确认组件与要使用的器身匹配,且选用适宜型号的穿刺器。不同厂家之间的微创腔镜类吻合器尺寸可能各不相同。一个手术中如果同时选用不同厂家生产的微创腔镜手术器械及其附件,在手术前要核实其是否兼容。
手术前放疗可能导致组织改变。例如,这些改变可能引起组织增厚而超过所选吻合钉的指定范围。任何对病人手术前的治疗都应经过仔细考量,可能需要更改手术技术或手术方式。
使用前必须检查吸塑包装有无破损,破损禁用。
器身的最大击发次数为5次,在同一台手术中一把器身最多可更换5次组件;
更换组件次数请勿超过最大击发次数。将吻合器与吻合线加固材料一起使用可能会使击发次数降低。
组件使用前必须确保保护盖封装完好,否则需检查组件内是否缺钉;且吻合器会发生装载故障。
退出器械后,务必检查缝合后组织是否有出血情况,如有渗血,须在相应部位电灼或缝补几针。
确保组织厚度在指定范围内、组织在吻合器内均匀分布。一侧组织过多可引起吻合不佳,可能会发生吻合口渗漏。
吻合钉高度选择参照如下:
◆A型钉仓(吻合钉高度为4.8mm)不能用于压缩后厚度小于2.5mm的组织。或不能适当地压缩到2.8mm厚度的组织及主动脉。
◆B型钉仓(吻合钉高度为3.5mm)不能用于压缩后厚度小于1.5mm的组织。或不能适当地压缩到2.0mm厚度的组织及主动脉。
◆E型钉仓(吻合钉高度为4.2)不能用于压缩后厚度小于2.0mm的组织。或不能适当地压缩到2.5mm厚度的组织及主动脉。
◆F型钉仓(吻合钉高度为4.0/4.5/5.0mm)不能用于压缩后厚度小于2.25mm的组织。或不能适当地压缩到3.0mm厚度的组织及主动脉。
◆G型钉仓(吻合钉高度为3.0/3.5/4.0mm)不能用于压缩后厚度小于1.5mm的组织。或不能适当地压缩到2.25mm厚度的组织及主动脉。
在组织过多或组织过厚的情况下,试图用力击发吻合器可能导致缝合线不完整,有可能吻合口裂开或渗漏。此外,可能发生器械损坏或击发失败。
击发必须一次性完成。切勿部分击发器械。不完全击发可能导致吻合钉成型不正常、切割线不完全、出血并从缝合线渗漏、和/或移除器械困难。、
在腹部手术过程中,如果不能形成并维持合适的气腹,可能会减少可用的操作空间,增加内脏组织伤害的危险。
MRI磁共振兼容性及限定使用条件:静态磁场强度小于或等于3T,空间磁场梯度不大于720-Gauss/cm。为时15分钟的MRI扫描过程中,人体的最大全身平均能量吸收率(SAR)不超过3.0W/kg。1.5T磁场环境下,吻合钉的射频致热最大温升不超过1.6℃;3T磁场环境下,吻合钉的射频致热最大温升不超过1.9℃。
本产品是灭菌包装,仅限同一台手术同一人使用。多名患者使用可能危及器械的完整性,或存在受污染的风险,进而可能会导致患者伤害。
本产品采用环氧乙烷(EO)灭菌,自灭菌之日起有效期为三年,内包装破损或过有效期禁止使用;生产日期、失效日期见合格证。
本产品严禁二次灭菌;
使用后请按规定销毁;
本说明书不可作为临床外科吻合技术指导使用的依据,有关临床外科吻合技术指导方面的问题,请参阅专业文献或咨询本公司及其代理商。
【禁忌症】
禁用于严重粘膜水肿。
禁用于主动脉。
如未提供近端或远端预防措施,请勿将腔镜切割吻合器用于大血管。
禁用于缺血或坏死组织。
禁用于肝脏或脾脏组织。这是由于此类组织的压缩特性,器械的闭合可能产生破坏性作用。
禁用于无法观察止血的部位。
不能用于禁用吻合钉的情况。
不能用于侧侧吻合手术。
不适用于无需取材活检的手术。
击发吻合器前,应评估组织厚度,如果组织无法轻松地压入吻合钉闭合高度或过于轻松地压入吻合钉闭合高度,则此组织不适合此吻合钉(可能过厚或过薄)。
【产品包装】
1、产品出厂时,内包装为吸塑盒无菌包装,外包装为纸盒,每盒一把,内附产品合格证和产品使用说明书。随货附出厂检验报告,过有效期或包装破损不得使用;
警告 不得二次 如包装破损 经环氧乙烷灭菌 无菌 查阅使用说明
使用 切勿使用
【产品保存】
贮存在相对湿度不大于80%无腐蚀性气体和通风良好的室内,应保证包装箱上的字样和标志不应历时较久而模糊不清。应防止撞击和挤压,放置于通风、干燥和无腐蚀性气体的室内。
【制造商】
生产企业/注册人/售后服务单位:常州市微凯医疗科技有限公司
住 所:江苏武进经济开发区长扬路9号
生产地址:江苏武进经济开发区长扬路9号(西太湖医疗产业孵化园C4幢二、三层及五层西边)
在线留言
如果您有任何建议,请留言或发邮件给我们,我们会在收到留言邮件后的1个工作日给您回复。



 产品咨询
产品咨询